乳腺癌(Breast Cancer, BC)作为最常见的女性恶性肿瘤,具有较强的肿瘤异质性。基底型乳腺癌(Basal Like Breast Cancer, BLBC)是乳腺癌中的一种特殊亚型,与三阴性乳腺癌(Triple Negative Breast Cancer, TNBC)具有相似特征,即:雌激素受体(Estrogen Receptor, ER)、孕激素受体(Progesterone Receptor, PR)和人表皮生长因子受体-2(Human Epidermal Growth Factor Receptor-2, HER2)表达均为阴性。BLBC具有侵袭性强,且预后不良等临床特征。因为靶点的选择性少,使得BLBC的临床用药一直存在着局限性,因此手术和放疗等局部治疗以及以化疗为基础的全身治疗仍是BLBC治疗的主要方式。
KLF5转录因子在BLBC中高表达,我们前期的研究表明,KLF5通过上调Cyclin D1、FGF-BP1、mPGES1和TNFAIP2的转录,下调细胞周期抑制因子p21和p27的转录,促进乳腺癌细胞周期的进展和肿瘤的生长。众所周知,Cyclin D1-CDK4/6复合物可磷酸化RB1并释放E2F转录因子,从而驱动G1/S细胞周期进程,与此一致,KLF5主要促进G1/S细胞周期的进展。然而,CDK4/6抑制剂在BLBC中没有表现出良好疗效的原因尚不清楚。
XPO1基因编码核输出蛋白1(Exportin 1)或染色体区域维持蛋白1(CRM1, XPO1)。它可以将至少221种具有核输出信号(NES)结构域的蛋白从细胞核转运到细胞质,如RB1、p53、p21、Beclin1和p27等肿瘤抑制因子。当RB1被运输出细胞核时,它不再能够抑制E2Fs释放和肿瘤细胞周期进程。此外,XPO1还可以在RNA结合蛋白的帮助下将mRNA、miRNA、rRNA等RNA转运出细胞核。XPO1在多种肿瘤中高表达,如小细胞肺癌、胶质瘤、胆管癌、肝癌等。据报道,XPO1抑制剂KPT-330(Selinexor)可抑制多发性骨髓瘤、弥漫性大B细胞淋巴瘤、结直肠癌和神经母细胞瘤细胞的增殖。此外,Selinexor已被批准用于骨髓瘤和弥漫性大B细胞淋巴瘤的临床治疗,疗效良好。有报道称,在BLBC患者中XPO1表达升高,KPT-330在BLBC细胞中具有抗肿瘤活性。KPT-330联合PI3K/mTOR抑制剂GSK2126458可以抑制BLBC肿瘤生长。在一项针对BLBC患者的Ib期临床试验中,Selinexor和Eribulin联合治疗具有更显著的疗效。此外,我们猜测CDK4/6抑制剂在BLBC中的疗效较差,原因可能是RB1磷酸化水平虽然受到抑制,但是BLBC中存在着的XPO1可以将RB1转运出核,这依旧会致使RB1的抑癌功能丢失。
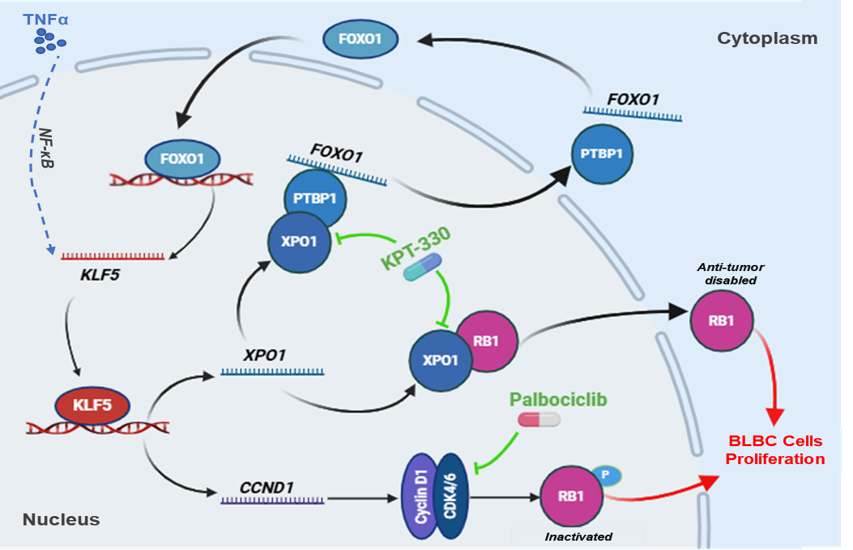
基于以上基础理论,乐鱼·(中国)集团有限公司,生物医学工程研究院的陈策实研究员团队发现了KLF5可通过诱导XPO1基因转录促进BLBC细胞增殖的新机制,XPO1也通过增加FOXO1的mRNA核输出,进而增加KLF5的表达。因此,在BLBC中形成了KLF5和XPO1之间的正反馈调节回路。同时,在BLBC中KLF5一方面促进CCND1(编码Cyclin D1蛋白)基因转录和RB1磷酸化,另一方面,KLF5促进XPO1基因转录和RB1核输出。这两种机制共同促进BLBC细胞内的RB1失活,导致细胞周期的进展加速。与此同时,研究表明XPO1抑制剂KPT-330和CDK4/6抑制剂Palbociclib联合使用可有效抑制BLBC细胞增殖和肿瘤生长。此研究结果表明XPO1可能是BLBC的潜在治疗靶点,同时,此研究为BLBC患者的临床治疗提供了一种新的联合用药策略。

2025年1月31日,以上研究成果以“Positive Feedback Regulation between KLF5 and XPO1 Promotes Cell Cycle Progression of Basal Like Breast Cancer”为题,在线发表于ADVANCED SCIENCE杂志(1区Top,五年影响因子14.3)。乐鱼·(中国)集团有限公司,生物医学工程研究院、乐鱼·(中国)集团有限公司,第三附属医院陈策实研究员、中国科学院昆明动物研究所蒋德伟研究员、武汉华中科技大学协和医院姚静教授为该论文的共同通讯作者。乐鱼·(中国)集团有限公司,第三附属医院唐余博士、刘睿博士,乐鱼·(中国)集团有限公司,生物医学工程研究院祝婧大创学生、何倩博士和乐鱼·(中国)集团有限公司,第一附属医院潘成隆博士为该论文的共同一作。该项工作得到了国家重点研发计划、国家自然科学基金、云南省云岭学者、云南省教育厅自然科学研究项目等的资助。
原文链接:http://doi.org/10.1002/advs.202412096
供稿:唐余;编校:张志毕;审核:陈亚娟、陈策实

